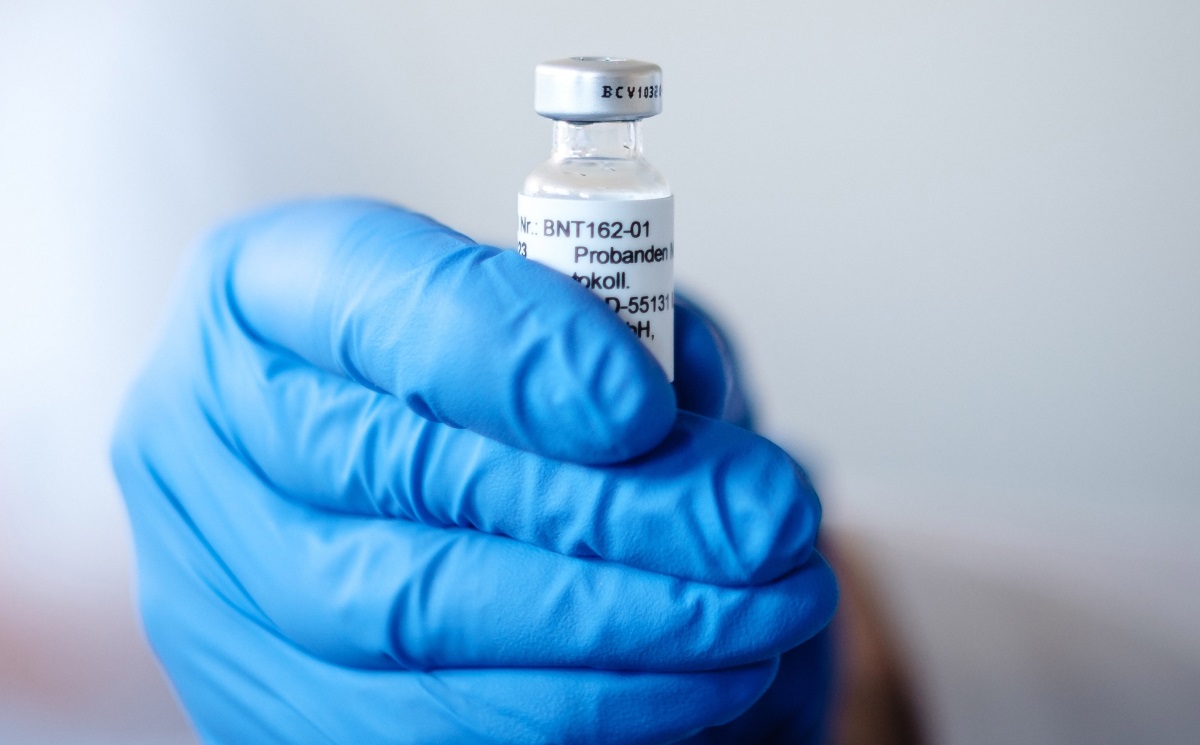
Az Európai Gyógyszerügynökség (EMA) javasolja, hogy ideiglenes forgalomba hozatali engedélyt kapjon a Pfizer–BioNTech gyógyszergyártók koronavírus elleni vakcinája, a 16 éven felüli lakosság számára – jelentette be Emer Cooke, az EMA ügyvezető igazgatója a szervezet amszterdami virtuális sajtótájékoztatóján. Ez az első oltóanyag, amely megkapja az uniós hatóság hozzájárulását. Most az Európai Bizottság feladata az engedély kiadása, erre nagyon rövid időn belül sor kerülhet.
Ursula von der Leyen bizottsági elnök már közölte, hogy ma este megteszi erre vonatkozó javaslatát. Így zöld utat kap az a terv, amely szerint december 27-én minden tagállamban meg lehet kezdeni az oltások beadását. Az Európai Bizottság összesen 200 millió adagra szerződött le ezzel a gyártóval, de további 100 millióra is bejelentette igényét. A dózisokat az egyes EU-országok népességük alapján osztják fel.
Az EMA szakértői biztonságosnak és hatékonynak értékelték a Pfizer–BioNTech oltást. Emer Cooke azt mondta, hogy „a tudományos bizonyítékok ereje és semmi más nem vezényelt bennünket”. Tudománytörténeti mérföldkőnek nevezte azt, hogy kevesebb mint egy éven belül sikerült oltást engedélyezni egy újfajta betegségre. Hozzátette, hogy nincs bizonyíték arra, hogy ne működne az új, Nagy-Britanniában felfedett változat esetében.
Ha minden a menetrend szerint halad, akkor a szállítmányok december 26-án hagyhatják el a raktárakat annak érdekében, hogy másnap megkezdődhessen az oltást.
A klinikai tesztek során kiderült, hogy az oltás 95 százalékban hatásos. Összesen több mint 44 ezer ember vett részt a kísérletben, akiknek fele a covidvakcinát, fele pedig placebót kapott. A Pfizer–BioNTech-injekcióval beoltott 18198 ember közül 8 kapta el később a koronavírust, az ellenszérumot nem kapó 18225 személy közül pedig 162 ember. A hatékonyság kimutatható volt a 75 éven felettiek, valamint a magas egészségügyi kockázatnak kitettek (asztmában, krónikus tüdőbetegségben, cukorbetegségben, magas vérnyomásban szenvedők, vagy túlsúlyosak) körében is.
A vakcinát két injekció formájában kell beadni a karba, legalább 21 napos különbséggel. A leggyakoribb mellékhatások általában enyhék vagy közepesek voltak, és az oltást követően néhány napon belül javultak. Megfigyelték az injekció beadásának helyén fellépő fájdalmat és duzzanatot, fáradtságot, fejfájást, izom- és ízületi fájdalmat, hidegrázást és lázat.